Autor: MV Diego Esteban Hernández
Virbac México
Introducción
La mastitis es una enfermedad de causas multifactoriales que ocasiona las mayores pérdidas económicas en la industria láctea, la mayoría de los casos de esta enfermedad es resultado de bacterias que llegan a colonizar la ubre, entrando a través del canal del pezón. En el contexto de la glándula mamaria bovina, la relación entre la vaca y los microorganismos ha sido visto tradicionalmente desde la perspectiva de la interacción del hospedero-patógeno, por medio de las infecciones intramamarias que ocasionan, presentándose de manera clínica o subclínica, de cualquier forma, la mastitis en las vacas lecheras es una enfermedad costosa debido a la reducción de la producción de leche, desvío de leche, costo de tratamientos, costos de mano de obra extra y sacrificio anticipado. Esta enfermedad debe prevenirse en lugar de curarse (Halasa et al. 2007; Soest et al. 2016).
Exposición a los patógenos de la mastitis
La exposición a los patógenos de la mastitis pueden originarse de varias fuentes, incluidas, el entorno de la vaca, infecciones intramamarias existentes anteriormente y flora de la piel del pezón (Pankey et al. 1989).
El score de higiene juega un papel fundamental, un alto nivel de suciedad incrementa el riesgo a desarrollar mastitis por patógenos medioambientales (Breen et al. 2009). Establos donde al menos el 50% de las vacas tienen un score de higiene de ubres de 3 o 4 aumenta un 1.49 más el riesgo de contraer una mastitis clínica causada por cualquier patógeno y 2.57 más riesgo de mastitis clínica causada por E. coli, que los establos donde menos del 50% de las vacas tenían un puntaje de higiene de la ubre de 3 o 4 (Verbeke et al. 2014). Conocer la flora microbiana de la piel del pezón es de suma importancia, ya que la probabilidad de una nueva infección intramamaria es altamente correlacionado con el número de patógenos causales de la mastitis en el extremo del pezón durante el ordeño (Pankey, et al., 1989).
Mecanismos de defensa bovina contra infecciones intramamarias
Inmunidad Innata
La respuesta inmune innata se caracteriza por una rápida activación que puede ocurrir segundos después de la exposición bacteriana, es la primera línea de defensa cuando la glándula mamaria se expone por primera vez a patógenos causantes de mastitis.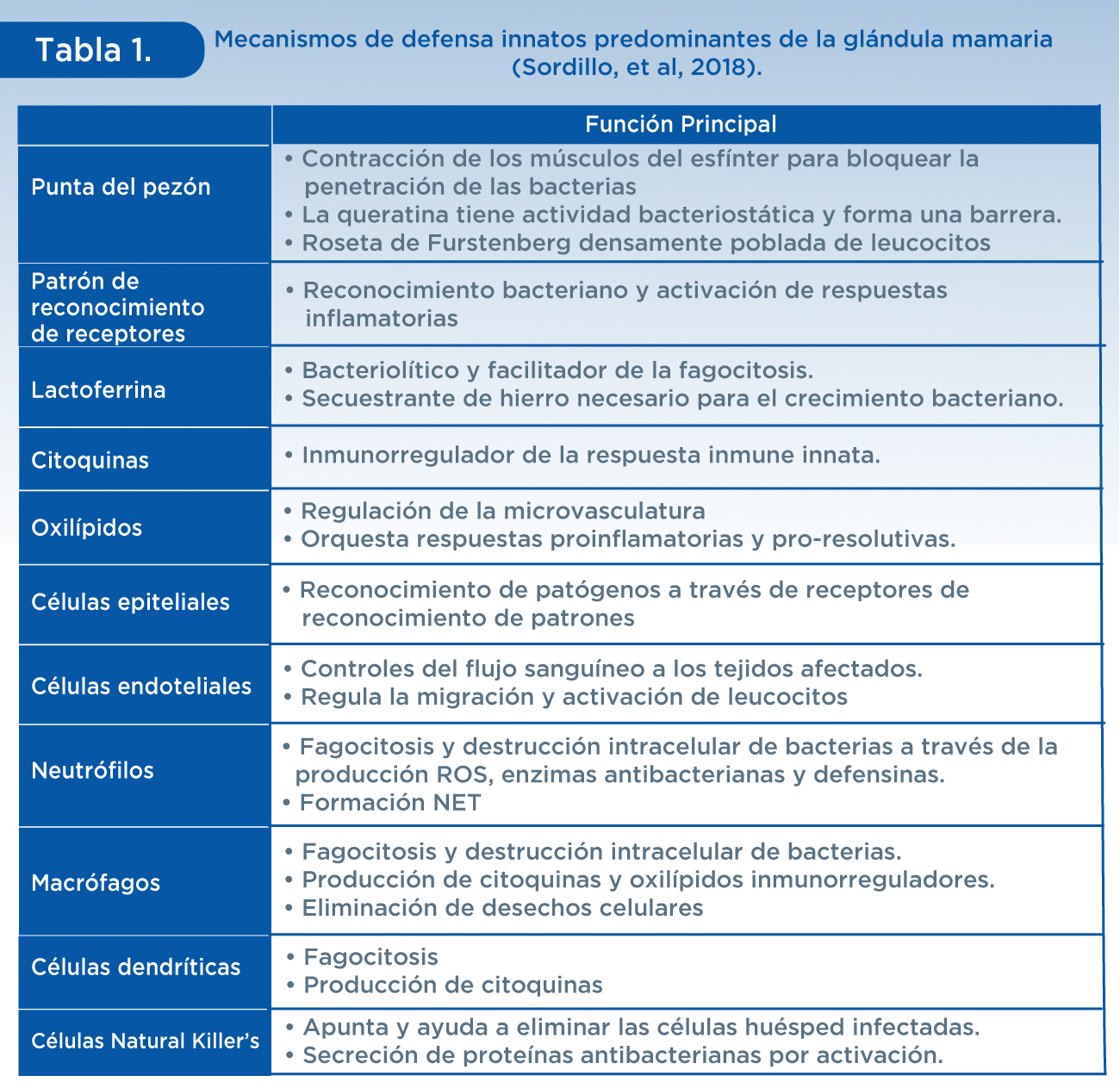
Reconocimiento del Patógeno
Cuando los patógenos causantes de mastitis penetran con éxito la punta del pezón, la capacidad de respuesta en presencia de bacterias dentro de la glándula mamaria es esencial para la inicio de la respuesta inmune innata. Las poblaciones de células mamarias localizadas son capaces de facilitar el reconocimiento de patógenos y puede estimular eficazmente los diversos procesos inmunes. Tanto las células inmunes y no inmunes en la glándula mamaria poseen Receptores de Reconocimiento de Patrones (PRR), identificando moléculas asociadas con patógenos microbianos, denominados Patrones Moleculares Asociados a Patógenos (PAMP). Ejemplos de estos PRR son los Receptores Tipo Toll (TLR), que son una familia de proteínas transmembranosas y están presentes en poblaciones de leucocitos, al igual que en células endoteliales, células epiteliales y fibroblastos que se distribuyen por los tejidos mamarios (Jungi, et al., 2011; Kumar, et al., 2010). Dentro de la familia TLR, Tanto TLR-2 como TLR-4 son de particular importancia para la defensa mamaria, ya que estos receptores reconocen los PAMP asociados con patógenos causantes de mastitis grampositivos (peptidoglicanos) y gramnegativos (lipopolisacáridos), incluyendo Staphylococcus aureus, Streptococcus uberis y Escherichia coli. (Goldammer et al., 2004; Porcherie, et al., 2012). Después del reconocimiento y la unión de patógenos a través de interacciones PRR-PAMP, se activan las vías de señalización, incluido el NFk-β, que controlar la expresión de varios mediadores solubles que desencadenan la cascada de la inflamación. (Liang, et al., 2004). La inflamación es un componente crítico del sistema de defensa innato que debe eliminar bacterias dentro de la glándula mamaria, ayudan con la reparación de cualquier daño tisular que puede ocurrir durante la invasión bacteriana, restaurando la estructura y función normal del tejido. Una eficiente respuesta inflamatoria de la glándula mamaria generalmente debe durar menos de una semana y no causar ningún cambio notable en la leche o los tejidos mamarios. La activación del NFk-β es una vía de señalización principal por la cual los mediadores solubles son producidos para impulsar el inicio de la cascada inflamatoria mamaria (Bannerman, et al., 2009; Boulanger, et al., 2003, Sordillo et al., 2018).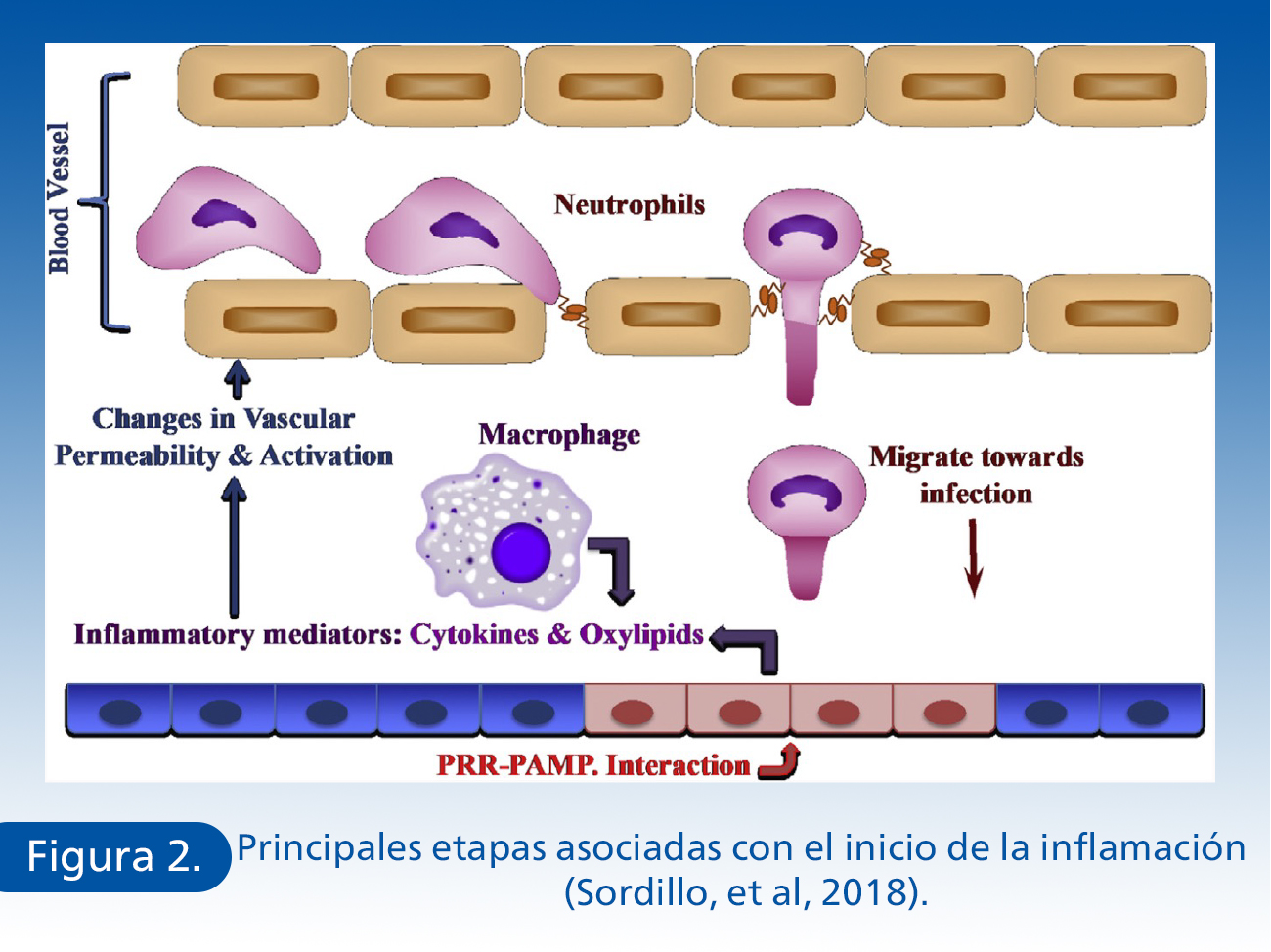
Programas de prevención y control de la mastitis
Mejorar la salud de las ubres al nivel de granja se basa en la aplicación de dos principios básicos:
- Reducción de la duración del infecciones intramamarias existentes.
- Reducir la incidencia de nuevos casos de mastitis mediante la prevención.
El Ordeño y la Salud del Pezón
Los efectos directos e indirectos de la máquina de ordeño pueden ocasionar hasta el 20% de incidencias de mastitis en algunos establos, y probablemente no más del 10% en un rebaño promedio en estos días (NMC 2017).
Una de las principales formas en que la máquina de ordeño influya en infecciones intramamarias es el riesgo a daños en la piel y punta de los pezones de las vacas, también tomando en cuenta la flora bacteriana que rodea la piel y punta de pezón, la preparación de las ubres al ordeño con el correcto uso de presello y sello, juega un papel fundamental, si no se llevan a cabo los debidos intervalos en la rutina de ordeño corremos el riesgo de incrementar la taza de incidencias de nuevas infecciones intramamarias de patógenos ambientales y patógenos contagiosos.
El ordeño es un contacto directo con los pezones de los animales, la selección de las pezoneras, el nivel de vacío y las pulsaciones impactan directamente sobre la condición de los pezones, y están correlacionados con el nivel de hiperqueratosis en las puntas de los pezones de la vacas (Zucali et al., 2008).
Uno de los factores determinantes para la condición del pezón es la fuerza del vacío aplicada durante el ordeño (Ohnstad, et al., 2012), esta fuerza de vacío en ocasiones siendo de manera prolongada o con vacíos de más de 44 kPa, afectan la primer barrera de defensa anatómica de la glándula mamaria, permitiendo mayor facilidad a patógenos a colonizar las ubres de las vacas (De Vliegher, et al., 2018). Para cada una de las pezoneras, el aumento de la presión de vacío ejerce de manera negativa una comprensión en los pezones haciendo que estos generen una cianosis y las puntas de los pezones empiecen a prolapsarse, estas variaciones de presión son los principales factores relacionados a la hiperqueratosis y prolapso de la punta del pezón (Zucali, et al., 2008).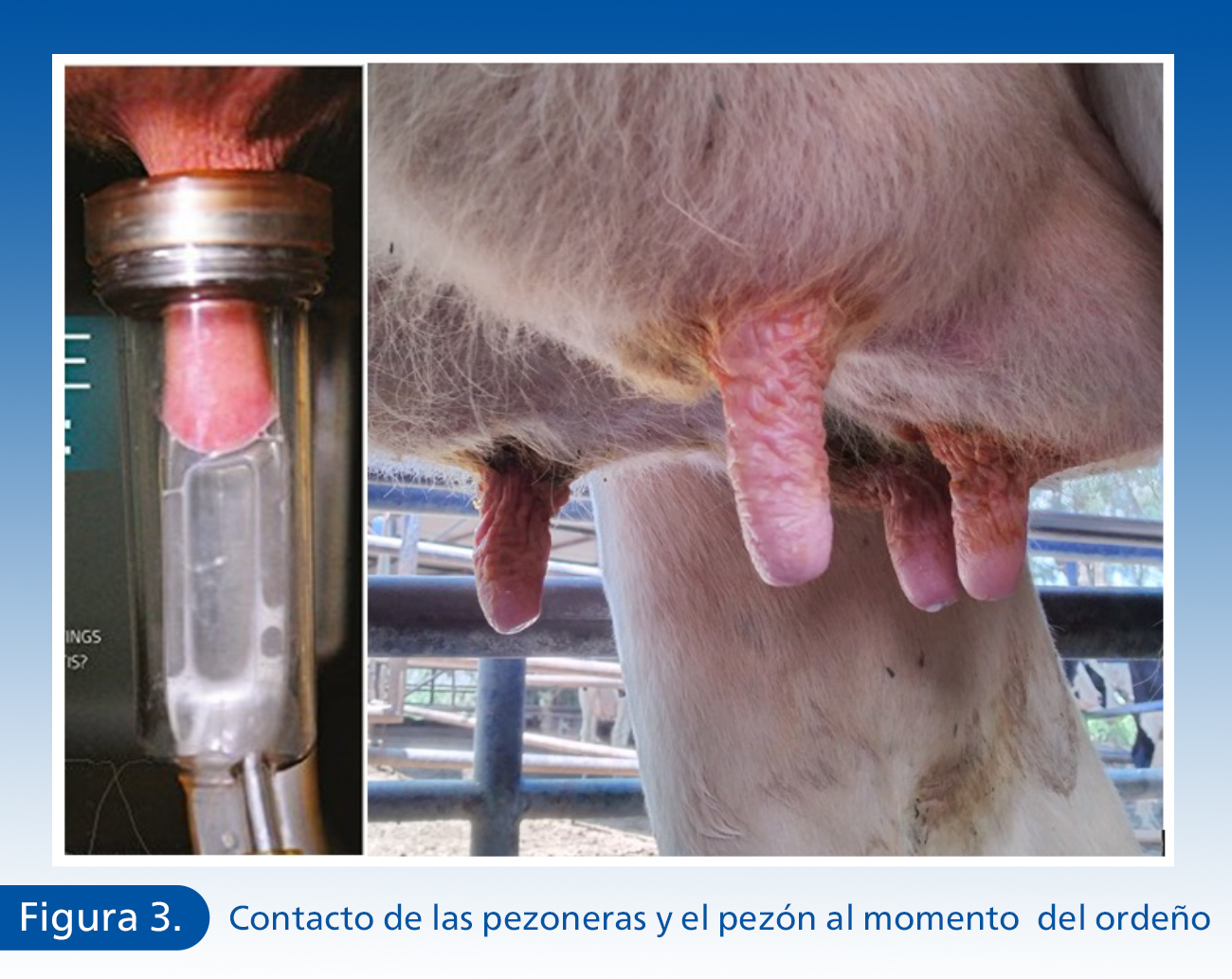
Una adecuada higiene del pezón pre ordeño disminuirá la cantidad de bacterias en la leche en el caso de que haya reflujo. Una buena estimulación del pezón 10 a 20 segundos, y un tiempo de espera de uno a dos minutos para colocar la unidad de ordeño luego de la estimulación, nos asegurará una buena bajada de leche y disminuirá el tiempo que la maquina está colocada en la ubre y evitar sobre ordeños. Es también muy importante mantener limpias las pezoneras (Ruegg, et al., 2005).
Camas y medio ambiente
Tomando en cuenta que las ubres y los pezones del ganado lechero pueden estar en contacto directo con materiales de las camas de un 40 a 60% del día, la exposición bacteriana en los echaderos puede ocasionar muchos problemas a la salud de la ubre dependiendo del nivel de humedad tengan y manejos realizados (Hogan y Smith et. al., 2012).
El cambio de arena nueva en camas, reduce drásticamente la exposición de las puntas de los pezones a los patógenos medioambientales de la mastitis en comparación con los materiales orgánicos (Hogan et al. 1989; Zdanowicz et al. 2004; Rowbotham y Ruegg et. al., 2016). Una desventaja importante de los subproductos orgánicos como aserrín, virutas de madera y paja, es su capacidad de albergar y cultivar patógenos de mastitis (Hogan y Smith et. al., 2012). En camas de estiércol a pesar del compostaje, recuentos bacterianos de patógenos de la mastitis han sido comparables en los días 2 y 6 con aquellos en estiércol fresco reciclado que fueron superiores (Cole y Hogan et. al., 2016). Los organismos son consistentes en diferentes tipos de camas incluyendo arena nueva, arena reciclada y sólidos de estiércol, con respecto a los colchones de goma con núcleo de espuma (Gao et al. 2017, De Vliegher, et al., 2018).

Mantenga siempre una cantidad adecuada de material de cama en los establos para proveer a las vacas una cama cómoda y seca. La limpieza y acondicionamiento de dichos establos debe realizarse de dos a tres veces por día para retirar el estiércol y el material húmedo. Para las camas de arena, es importantísimo que los 60 a 90 cm posteriores del mismo sean limpiados y nivelados en cada ordeño. Para los establos a corrales libres, realice un cronograma semanal de reemplazo de la arena, así se asegurará que estarán cómodos y limpios (Ruegg, et al., 2005).
Cambio de manejos basados en los datos del establo
El conteo de células somáticas en leche de tanque es determinado por el porcentaje de vacas con una elevación recuento de células somáticas >200 000 células/ml.
Uno debe esforzarse para obtener una tasa de curación de más del >40% por mes en aquellas vacas con mastitis clínica, esto puede ser traducido a una tasa promedio de infección de 2% al mes del hato total. Uno debe luchar por menos de ≤10% lo que respecta infecciones intramamarias crónicas.
Las Infecciones de la glándula mamaria son causadas por agentes bacterianos de tipo contagiosos o ambientales. Patógenos como Staphylococcus aureus y Streptococcus agalactiae dentro de los clasificados como contagiosos, necesitan un hospedero para sobrevivir y multiplicarse. A diferencia de los patógenos medioambientales u oportunistas como Streptococcus uberis y Escherichia coli, que no necesitan un hospedero para sobrevivir y multiplicarse.
Una alta tasa de incidencias de mastitis causados por patógenos medioambientales sugieren una mala higiene en áreas donde descansan las vacas, una de las herramientas más útiles en el combate a las mastitis son los cultivos bacteriológicos de leche a nivel de tanque, pool’s de vacas con mastitis dentro del establo y de vacas individuales, esto nos permite determinar el agente patógeno causal del problema, ya sea un contagioso como Streptococcus agalatiae, Mycoplasma spp., o un agente medioambiental como es el caso de Streptococcus uberis y E. coli (Zadoks et al., 2005).
En el manejo de la terapia de secado, si nuestros resultados son más del >15% de vacas frescas con elevados conteos de células somáticas, indican que demasiadas vacas contrajeron una nueva infección intramamaria dentro del período seco o no se curó con éxito de una infección existente desde la lactancia anterior (Barkema et al. 2013).
En varias encuestas de mastitis realizadas al nivel mundial, las vaquillas albergan una prevalencia de infecciones intramamarias al momento del parto de un 60% trimestrales (De Vliegher et al. 2018).
Una alta incidencia de mastitis clínica (≥2% por mes) podría ser el resultado de un alto porcentaje de primeros casos de mastitis clínica (≥10%), o un alto porcentaje de casos de mastitis reincidente (> 30%), o ambos. Considerar que los cuartos que tuvieron al menos un caso de mastitis clínica durante la lactancia previa, tienen 4.2 veces más probabilidades de reincidir en una mastitis clínica en la lactancia actual (Pantoja et al. 2009). En vacas multíparas hay mayor riesgo de un segundo caso de mastitis clínica causado por el mismo agente patógeno que causo el primero (Cha et al. 2016).
Una alta tasa de reincidencia puede que sea debido a:
- Problemas con las infecciones por Staphylococcus aureus que pueden ser Difícil de eliminar.
- Mala inmunidad, dificultando la eliminación de la infección.
- Elección incorrecta de tratamiento, por ejemplo, duración muy corta o antibiótico incorrecto.
- Mala detección de mastitis donde estas no se detecta rápidamente y oportunamente.
Para lograr y mantener una buena salud de ubre en el hato lechero, es bien conocido el programa de los 10 puntos del control y la prevención de la mastitis (NMC 2017). Es importante analizar y encontrar el problema primero, luego ofrecer una solución efectiva basada en evidencia para cada problema específico del hato, basada en hechos e información (Barkema et al. 2013). La medición individual del conteo de células somáticas por medio de una prueba california de las vacas de forma regular (es decir, cada 4 a 6 semanas), así como un preciso y detallado registro de las mastitis clínica es indispensable para mejorar y controlar la salud de las ubres en un establo lechero. (De Vliegher, et al., 2018).
BIBLIOGRAFIA
De Vliegher, Sarne. Ohnstad, Ian. Piepers, Sofie. “Management and prevention of mastitis: A multifactorial approach with a focus on milking, bedding and data-management”. Journal of Integrative Agriculture 2018, 17(6): 1214–1233
Sordillo, L. M. “Mammary gland immunobiology and resistance to mastitis”. Veterinary clinics: food Animal Practice, 2018, 34(3), 507-523.
Alnakip, Mohamed. Quintela-Baluja, Marcos. “The Immunology of Mammary Gland of Dairy Ruminants between Healthy and Inflammatory Conditions”. Journal of Veterinary Medicine. 2014, Article ID 659801, 31 pages.
Paduch J H, Mohr E, Kromker V. 2013. “The association between bedding material and the bacterial counts of Staphylococcus aureus, Streptococcus uberis and coliform bacteria on teat skin and in teat canals in lactating dairy cattle”. Journal of Dairy Research, 80, 159–164.
NMC (National Mastitis Council, A global organization for mastitis control and milk quality). 2017. “Current Concepts of Bovine Mastitis”. 5th ed. National Mastitis Council, New Prague, Minnesota, United States.




Deja un comentario